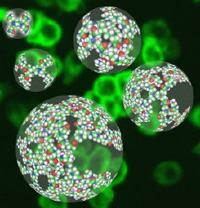
La utilización de nanotecnologia en el ámbito de la medicina nos permitirá abordar con éxito la cura de muchas enfermedades. En la Universidad de California han comenzado a utilizar nanopartículas mesoporosas de sílice como vehículo para superar el problema de la insolubilidad en agua de muchos fármacos anticáncer, aumentando su eficacia.
Cuando hablamos de nanomáquinas, es posible que imaginemos una especie de vehiculo en miniatura, dotado de algún tipo de piloto automático, capaz de llevar a cabo tareas complejas dentro del cuerpo humano (u otro entorno). Sin embargo, la nanotecnologia puede ser sumamente útil sin necesidad de semejante complejidad. El secreto de su éxito es, por supuesto, el pequeño tamaño de sus componentes.
Uno de los problemas mas graves de las terapias anticáncer basadas en medicamentes reside en la pobre solubilidad en agua que tienen estos fármacos anticancerígenos. Para que puedan realizar su labor, deben ser tratados con sustancias que los ayuden a disolverse luego de ser ingeridos para que puedan ser absorbidos por las células cancerosas. Pero el agregado de estos disolventes no sólo disminuye la potencia y eficacia de los medicamentos sino que también producen efectos tóxicos indeseados en el paciente.
Con este problema en mente, investigadores pertenecientes al Instituto Californiano de Nanosistemas, que depende de la Universidad de California (UCLA); y al Centro Oncológico Jonsson, desarrollaron unas nanopartículas compuestas de sílice que permiten a los medicamentes oncológicos (como la camptotecina, entre otros) ser fácilmente disueltos y mejorar su eficacia a la hora de atacar las células cancerosas humanas.
Los científicos a cargo de la dirección del proyecto son Fuyu Tamanoi, un profesor de microbiología, inmunología y genética molecular que se desempeña en la UCLA, y Jeffrey Zink, profesor de química y bioquímica en la misma institución. Juntos crearon un método que ha resultado ser eficaz para resolver el problema de la solubilidad. Básicamente, se trata de incorporar las moléculas del medicamento en cuestión en los “poros” que presenta la superficie de algunas nanopartículas, convirtiéndolas en una especie de “medio de transporte” para la droga.
Zink y Tamanoi trabajaron con nanopartículas mesoporosas fluorescentes de sílice, cargadas con moléculas del medicamento anticancerígeno hidrófobo camptotecina. Una vez introducidas en el cuerpo, las moléculas de camptotecina son liberadas y pueden adosarse a las diversas células cancerosas humanas para inducirles la muerte celular. Los resultados disponibles son alentadores, y sugieren que las nanopartículas mesoporosas de sílice podrían utilizarse como un vector de transporte mucho menos toxico que los diluyentes empleados actualmente por los fármacos anticáncer.
Las nanopartículas empleadas son biocompatibles. Su superficie contiene una gran cantidad de poros tubulares en los que se alojan los medicamentos a distribuir, y lo mejor de todo, son relativamente fáciles de modificar para adaptarla a nuevas “misiones”. Los científicos apuestan al desarrollo de estas nanopartículas debido al claro potencial que han demostrado para convertirse en un sistema biocompatible y eficiente de liberación de medicamentos.
En este momento, se considera que la camptotecina y sus derivados como los medicamentos anticancerígenos mas eficientes. Diferentes experimentos realizados en laboratorios han demostrado que son efectivos contra los carcinomas de estómago, colon, cuello, vejiga, cáncer de mama, de pulmón (de células pequeñas) y la leucemia. Pero a la hora de aplicarlos a un paciente humano, solo pueden utilizarse derivados de la camptotecina que sean solubles en agua, que generalmente son mucho menos eficaces.
Este problema se ha encarado con métodos convencionales, como liberación mediante el empleo de ciertos polímeros y partículas liposomales. Pero el empleo de nanopartículas de sílice mesoporosas ha mostrado un gran potencial, y constituyen el método más prometedor para la liberación de agentes terapéuticos en puntos precisos de órganos (o incluso de grupos pequeños de células) seleccionados como objetivos.